
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、C2H2 |
| B、C2H4 |
| C、C2H6 |
| D、C3H6 |
查看答案和解析>>
科目: 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目: 来源: 题型:
| 名称 | 托盘天平 | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  | |
| 序号 | a | b | c | d | e | f |
| 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目: 来源: 题型:
| A、①② | B、③④⑤ |
| C、③⑤ | D、①③④ |
查看答案和解析>>
科目: 来源: 题型:
| 物质 | H2 | CO | CH4 |
| 燃烧热kJ?mol-1 | 285.8 | 283.0 | 890.3 |
查看答案和解析>>
科目: 来源: 题型:
| A、M、N、Q三种物质的浓度一定相等 |
| B、M、N全部变成了Q |
| C、反应物和生成物的浓度都保持不变 |
| D、反应已经停止 |
查看答案和解析>>
科目: 来源: 题型:
A、 I2(g)+H2(g)?2HI(g) |
B、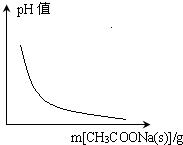 CH3COOH?H++CH3COO-(忽略溶液体积变化) |
C、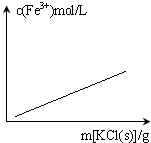 FeCl3+3KSCN?Fe(SCN)3+3KCl(忽略液体体积变化) |
D、 CH3OCH3(g)+3H2O(g)?6H2(g)+2CO(g)-Q(恒压) |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com