
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、制备硫酸亚铁铵的实验中最后制得的晶体过滤后用蒸馏水洗涤 |
| B、AgI 沉淀中滴入稀KCl溶液,有白色沉淀出现,说明AgCl比AgI更难溶 |
| C、倾析法是将不溶物充分沉淀后,先转移沉淀后转移液体 |
| D、配制好的氢氧化钠溶液用邻苯二甲酸氢钾滴定浓度时,采用酚酞为指示剂 |
查看答案和解析>>
科目: 来源: 题型:
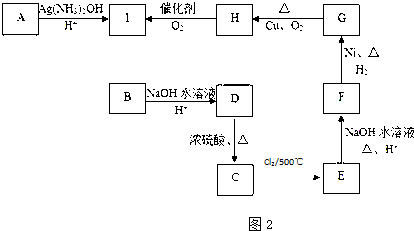
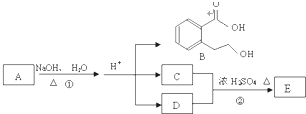 如图中 A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物.
如图中 A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| Mg |
| 无水乙醚 |

查看答案和解析>>
科目: 来源: 题型:
| △ |
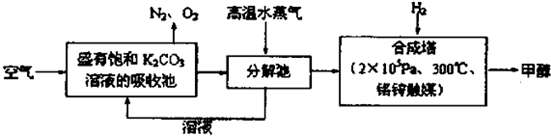
 ,物质A在体内脱氢酶的作用下会氧化为有害物质GHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.
,物质A在体内脱氢酶的作用下会氧化为有害物质GHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.
 结构),它的结构简式为
结构),它的结构简式为查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| A、60 mL |
| B、40mL |
| C、30 mL |
| D、15 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com