
科目: 来源: 题型:
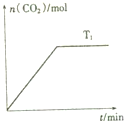 已知:反应①②③的平衡常数(K)与反应热(△H)的部分相关数据如表所示.
已知:反应①②③的平衡常数(K)与反应热(△H)的部分相关数据如表所示.| 反应 | 平衡常数(K) | 反应热(△H) | |
| 900℃ | 1100℃ | 900℃ | |
| ①Fe(s)+CO2(g) FeO(s)+CO(g) | 1.98 | 2.15 | akJ/mol |
| ②Fe(s)+H2O(g) FeO(s)+H2(g) | 1.98 | 1.47 | |
| ③CO(g)+H2O(g)CO2(g)+H2(g) | ckJ/mol | ||
查看答案和解析>>
科目: 来源: 题型:
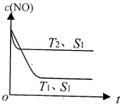 (1)汽车内燃机工作时发生反应:N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向5L密闭容器中充入6.5molN2和7.5molO2,在5min时反应达到平衡状态,此时容器中NO的物质的量是5mol.
(1)汽车内燃机工作时发生反应:N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向5L密闭容器中充入6.5molN2和7.5molO2,在5min时反应达到平衡状态,此时容器中NO的物质的量是5mol.查看答案和解析>>
科目: 来源: 题型:
 现有氨水、醋酸、盐酸、氯化铵四种溶液,请回答下列问题:
现有氨水、醋酸、盐酸、氯化铵四种溶液,请回答下列问题:| C(NH3?H2O) |
| C(OH-) |
查看答案和解析>>
科目: 来源: 题型:

 ) 合成路线的一部分.现在人们利用最新开发的+2价钯的均相钯催化剂体系,将丙炔在甲醇和一氧化碳存在下,于60℃、6MPa条件下羰基化,一步制得
) 合成路线的一部分.现在人们利用最新开发的+2价钯的均相钯催化剂体系,将丙炔在甲醇和一氧化碳存在下,于60℃、6MPa条件下羰基化,一步制得  ,其化学方程式为:
,其化学方程式为: .
. ,模仿以上流程图设计合成路线,标明每一步的反应物及反应条件.(有机物写结构简式,其它原料自选)
,模仿以上流程图设计合成路线,标明每一步的反应物及反应条件.(有机物写结构简式,其它原料自选)| 浓硫酸 |
| 170℃ |
| 高温、高压 |
| 催化剂 |
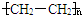 .
.查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
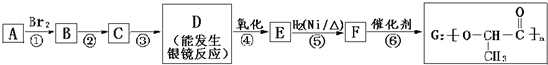
 肉桂醛F(化学式为C9H8O )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
肉桂醛F(化学式为C9H8O )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:查看答案和解析>>
科目: 来源: 题型:
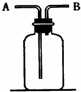 根据正放在桌面上的如图装置,回答下列问题:
根据正放在桌面上的如图装置,回答下列问题:查看答案和解析>>
科目: 来源: 题型:
| n |
| 2 |

查看答案和解析>>
科目: 来源: 题型:
 某化学课外活动小组应用如图所示的方法研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气,回答下列问题.
某化学课外活动小组应用如图所示的方法研究物质的性质,其中气体X的主要成分是氯气,杂质是空气和水蒸气,回答下列问题.查看答案和解析>>
科目: 来源: 题型:
 如图所示,烧杯内装有蒸馏水,下部封有半透膜的长颈漏斗内装有淀粉和食盐溶液,漏斗颈内的液面略高于烧杯内蒸馏水的液面,过一段时间后用碘水和硝酸银溶液分别检验蒸馏水中的物质.整个实验过程中,所观察到的现象是( )
如图所示,烧杯内装有蒸馏水,下部封有半透膜的长颈漏斗内装有淀粉和食盐溶液,漏斗颈内的液面略高于烧杯内蒸馏水的液面,过一段时间后用碘水和硝酸银溶液分别检验蒸馏水中的物质.整个实验过程中,所观察到的现象是( )| A、漏斗颈内液面下降 |
| B、漏斗颈内液面上升 |
| C、烧杯内液体遇硝酸银溶液没有白色沉淀生成 |
| D、烧杯内液体遇碘水变蓝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com