
科目: 来源: 题型:
| A、合成氨工业中,将NH3及时液化分离有利于加快反应速率 |
| B、氯碱工业中,使用离子交换膜可防止Cl2和NaOH溶液反应 |
| C、硫酸工业中,接触室内安装热交换器,是为了利用沸腾炉中排出的SO2的热量 |
| D、硫酸工业中,SO2的催化氧化不采用高压,是因为压强对SO2转化率无影响 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、以O2浓度变化表示的反应速率为0.064 mol?(L?s)-1 | ||
| B、反应达到平衡状态时NH3的转化率为20% | ||
C、升高温度能使
| ||
| D、将容器的体积变为4 L,平衡时NO的浓度小于0.4 mol?L-1 |
查看答案和解析>>
科目: 来源: 题型:
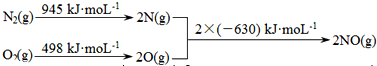
| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目: 来源: 题型:
| A、“水滴石穿”可能的原因是溶解了CO2的雨水与CaCO3作用生成了可溶性Ca(HCO3)2的缘故 |
| B、25℃时,难溶物XY和AB3的Ksp分别为1.0×10-10和2.7×10-15,则该温度下,两者的饱和溶液中c(X+)一定大于c(A3+) |
| C、25℃时,pH=ll的KaA溶液和pH=11的KOH溶液,水电离的c(OH-)前者是后者的108倍 |
| D、不用其它试剂能把NaCl、AlCl3、Ba(OH)2三种溶液鉴别出来 |
查看答案和解析>>
科目: 来源: 题型:
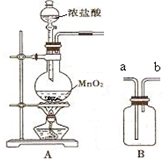 实验室用如图所示装置A、B进行组合制取氯气,按要求回答下列问题:
实验室用如图所示装置A、B进行组合制取氯气,按要求回答下列问题:| 实验目标 | 装填试剂 (填选项字母) | 气体流向 (填a、b) |
| 除去HCl杂质 | E | a→b |
| 干燥氯气 | C | a→b |
| 收集氯气 | D | |
| 检验氯气的氧化性 | F |
查看答案和解析>>
科目: 来源: 题型:
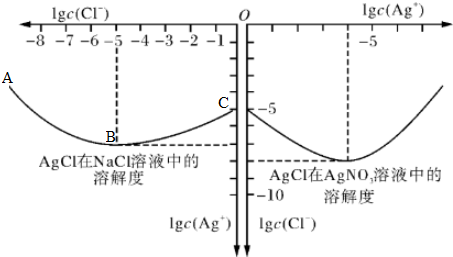
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com