
科目: 来源: 题型:
A、氨气:N2+3H2
| ||||
B、铝:2Al2O3(熔融)
| ||||
C、氯气:MnO2+4HCl(浓)
| ||||
D、硫酸:2SO2+O2
|
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| A、13g | B、9.75g |
| C、6.5g | D、3.25g |
查看答案和解析>>
科目: 来源: 题型:
| 组别 | 药品1 | 药品2 | 实验现象 |
| Ⅰ | 0.1mol?L-1NaOH溶液 | 0.1mol?L-1MgCl2溶液 | 生成白色沉淀 |
| Ⅱ | 0.1mol?L-1氨水 | 0.1mol?L-1MgCl2溶液 | 无现象 |
| Ⅲ | 1mol?L-1氨水 | 1mol?L-1MgCl2溶液 | 现象III |
| Ⅳ | 1mol?L-1氨水 | 0.1mol?L-1MgCl2溶液 | 生成白色沉淀 |
| Ⅴ | 0.1mol?L-1氨水 | 1mol?L-1MgCl2溶液 | 无现象 |
查看答案和解析>>
科目: 来源: 题型:
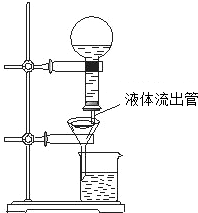 某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”,如图所示.在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗.为使液体顺利流下,还需插入“空气导入管”与大气相通.
某学生为了使过滤操作能自动添加液体,设计了“自动加液过滤器”,如图所示.在倒置的烧瓶中盛放待过滤的液体,液体从“液体流出管”流入漏斗.为使液体顺利流下,还需插入“空气导入管”与大气相通.查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
 研究NO2、SO2、NO、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、NO、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
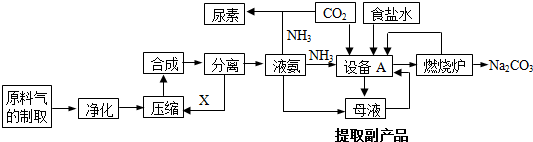
 向下列各组物质的混合溶液中滴加NaOH溶液,其现象与图象描述一致的是( )
向下列各组物质的混合溶液中滴加NaOH溶液,其现象与图象描述一致的是( )| A、HCl和Ba(NO3)2 |
| B、CuSO4和H2SO4 |
| C、CuSO4和Na2SO4 |
| D、Na2SO4和Ba(NO3)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com