
科目: 来源: 题型:
| 实验序号 | 实验内容 | 实验结果 |
| ① | 第一份中加AgNO3溶液 | 有白色沉淀生成 |
| ② | 第二份中加足量NaOH溶液并加热 | 只收集到标准状况下0.896L气体,无沉淀生成,同时得到溶液A |
| ③ | 向溶液A中通入过量CO2,所得白色沉淀经过滤、洗涤、灼烧后称量 | 固体质量为2.04g |
| ④ | 第三份加足量BaCl2溶液,所得沉淀经足量稀盐酸洗涤、干燥后称量 | 沉淀质量为23.3g |
| 阴离子符号 | 物质的量浓度(mol?L-1) |
查看答案和解析>>
科目: 来源: 题型:
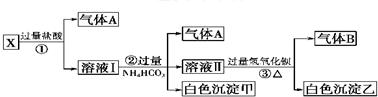
| A、气体A能使湿润的红色石蕊试纸变蓝,气体B能使湿润的蓝色石蕊试纸变红 |
| B、白色沉淀甲是混合物,白色沉淀乙是纯净物 |
| C、Ag+、Ba2+、Al3+、MnO4-、SO42-一定都不存在于溶液中 |
| D、Na+、AlO2-、CO32-一定存在于溶液中 |
查看答案和解析>>
科目: 来源: 题型:
 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯.回答下列问题:查看答案和解析>>
科目: 来源: 题型:
 实验室用如图装置制取乙酸乙酯.
实验室用如图装置制取乙酸乙酯.查看答案和解析>>
科目: 来源: 题型:
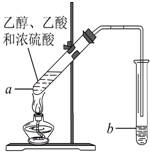 在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.查看答案和解析>>
科目: 来源: 题型:


| 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目: 来源: 题型:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
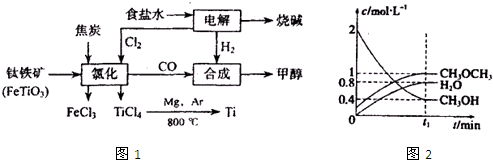
| ||
查看答案和解析>>
科目: 来源: 题型:

| A、以酚酞为指示剂,溶液颜色发生突变时(b点),Na2CO3转化为NaHCO3 |
| B、以甲基橙为指示剂,溶液颜色发生突变时,共消耗盐酸20.00ml |
| C、溶液pH=7(c点),碳酸钠完全转化为NaCl |
| D、ce段对应溶液中CO2与NaHCO3共存 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com