
科目: 来源: 题型:
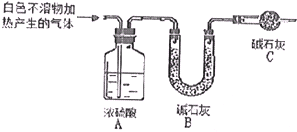 某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.
某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.查看答案和解析>>
科目: 来源: 题型:
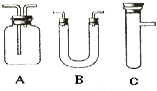 浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C
浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C
| ||
| 选用的仪器 (填字母) | 加入的试剂 | 作用 |
| C | 浓H2SO4、木炭 | 发生反应 |
| B | 检验产物水 | |
| A | 检验SO2 | |
| A | 酸性KMnO4溶液 | |
| A | 品红 | |
| A | 检验CO2的存在 |
查看答案和解析>>
科目: 来源: 题型:

| A、固体混合物中一定含有Al,但质量不可确定 |
| B、固体混合物中一定不含有AlCl3 |
| C、固体混合物中一定含有MgCl2和FeCl2 |
| D、固体混合物中一定含有 (NH4)2SO4和MgCl2,且物质的量之比为1:1 |
查看答案和解析>>
科目: 来源: 题型:
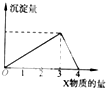 将X气体(或溶液)慢慢通入(或加人)一定量的Y溶液中,产生沉淀量与加入X的物质的量(mol)的关系如图所示,符合如图情况的是( )
将X气体(或溶液)慢慢通入(或加人)一定量的Y溶液中,产生沉淀量与加入X的物质的量(mol)的关系如图所示,符合如图情况的是( )| A、X为NaOH溶液,Y为AlCl3溶液 |
| B、X为CO2,Y为Ca(OH)2溶液 |
| C、X为NH3,Y为AlCl3溶液 |
| D、X为HCl溶液,Y为Na[Al(OH)4]溶液 |
查看答案和解析>>
科目: 来源: 题型:
| A、0.5 mol |
| B、0.25 mol |
| C、0.15 mol |
| D、1 mol |
查看答案和解析>>
科目: 来源: 题型:
| ||
| ||
| A、②和③ | B、仅有③ |
| C、仅有④ | D、以上都错 |
查看答案和解析>>
科目: 来源: 题型:
| 滴入KMnO4溶液的次序 | KMnO4溶液紫色褪去所需的时间 |
| 先滴入第1滴 | 60s |
| 褪色后,再滴入第2滴 | 15s |
| 褪色后,再滴入第3滴 | 3s |
| 褪色后,再滴入第4滴 | 1s |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
- 2 |
查看答案和解析>>
科目: 来源: 题型:
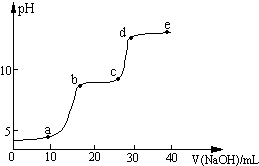 某研究性学习小组拟探究在含Mg2+、Al3+的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程.在0.1mol?L-1 MgSO4、0.05mol?L-1 Al2(SO4)3的混合溶液中滴加0.5mol?L-1 NaOH溶液,借助氢离子传感器和相应分析软件,测得溶液的pH随NaOH溶液的加入变化情况如图所示.
某研究性学习小组拟探究在含Mg2+、Al3+的混合溶液中滴加NaOH溶液时,生成氢氧化物沉淀的过程.在0.1mol?L-1 MgSO4、0.05mol?L-1 Al2(SO4)3的混合溶液中滴加0.5mol?L-1 NaOH溶液,借助氢离子传感器和相应分析软件,测得溶液的pH随NaOH溶液的加入变化情况如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com