
科目: 来源: 题型:
| A、不能,因为已经变质 |
| B、不能,因为含有杂质 |
| C、不能,因为含有水份 |
| D、能,因为那只是油脂主要成份在低温下结晶析出,是正常物理形态变化,并未变质 |
查看答案和解析>>
科目: 来源: 题型:
| A、①② | B、①④ | C、①③ | D、②③ |
查看答案和解析>>
科目: 来源: 题型:
| A、用FeCl3溶液腐蚀铜箔制作印刷电路板:Fe3++Cu═Cu2++Fe2+ |
| B、用Na2CO3溶液处理水垢中的CaSO4:CO32-+CaSO4?CaCO3+SO42- |
| C、碳酸钠溶液显碱性:CO32-+2H2O═H2CO3+2OH- |
| D、用NaOH溶液吸收氯气:Cl2+2OH-═2Cl-+H2O |
查看答案和解析>>
科目: 来源: 题型:
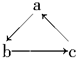 硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示).下列说法错误的是( )
硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如图所示).下列说法错误的是( )
| A、碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂 |
| B、常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大 |
| C、可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D、为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
查看答案和解析>>
科目: 来源: 题型:

| A、除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B、在过程②中将MgCl2?6H2O灼烧即可制得无水MgCl2 |
| C、从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| D、从第③步到第⑤步的目的是为了浓缩 |
查看答案和解析>>
科目: 来源: 题型:
| A、平衡向正反应方向移动了 |
| B、物质A的转化率增大了 |
| C、恒温恒压时再充入A物质,达到新的平衡时A的质量分数增加了 |
| D、a>b |
查看答案和解析>>
科目: 来源: 题型:
| A、78g 苯含有C=C双键的数目为3NA |
| B、室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| C、0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA |
| D、含2molH2SO4的浓硫酸与足量铜片在加热条件下反应,一定能产生NA个SO2气体分子 |
查看答案和解析>>
科目: 来源: 题型:
| A、2C2H2(g)+502(g)=4C02 (g)+2H20 (1)△H=-2b kJ.mol-l | ||
B、C2H2(g)+
| ||
| C、2C2H2(g)+502(g)=4C02 (g)+2H20 (1)△H=-4b kJ.mol-l | ||
| D、2C2H2(g)+502(g)=4C02 (g)+2H20 (1)△H=b kJ.mol-l |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com