
科目: 来源: 题型:
| 主族 周期 | IA | IIA | IIIA | IV A | V A | VI A | VII A | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
查看答案和解析>>
科目: 来源: 题型:
| ||
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 3 |
查看答案和解析>>
科目: 来源: 题型:
| 实验操作 | 实验现象 | 化学方程式 |
| 1、将少量氯水加入盛有 NaBr溶液的试管中,用力振荡后加入少量CC14,振荡、静置 | 溶液分层 上层: 下层: | ① |
| 2、将少量氯水加入盛有 KI溶液的试管中,用力振荡后加入少量CC14,振荡、静置 | 溶液分层 上层: 下层: | ② |
| 3、将少量溴水加入盛有 KI溶液的试管中,用力振荡后加入少量CC14,振荡、静置 | 溶液分层 上层: 下层: | ③ |
| 实验结论 | 卤族单质CI2、Br2、I2的氧化性强弱顺序为: | |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
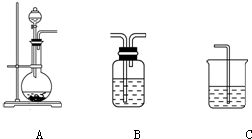 (1)下列实验操作或对实验事实的描述正确的有
(1)下列实验操作或对实验事实的描述正确的有| 气体 | O2 | Cl2 | NH3 |
| 分液漏斗中试剂 | H2O | 浓氨水 | |
| 圆底烧瓶中试剂 | KMnO4 |
查看答案和解析>>
科目: 来源: 题型:
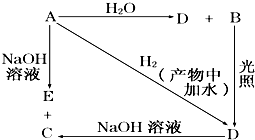 常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系如图所示.
常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系如图所示.查看答案和解析>>
科目: 来源: 题型:
| 压强MPa 转化率% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com