
科目: 来源: 题型:
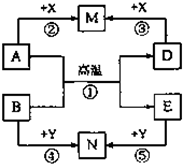 构建知识网络是学习化学的重要方法.下列物质的转化网络可以概括几类反应,其中A、B、D、E、M、N、X、Y均表示一种中学化学中常见的无机物,反应②、③、④、⑤的生成物可以是一种或几种.请回答下列问题:
构建知识网络是学习化学的重要方法.下列物质的转化网络可以概括几类反应,其中A、B、D、E、M、N、X、Y均表示一种中学化学中常见的无机物,反应②、③、④、⑤的生成物可以是一种或几种.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:
 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:查看答案和解析>>
科目: 来源: 题型:
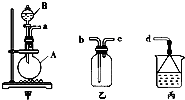 化学是一门以实验为基础的科学,熟练使用中学化学实验中的常见仪器,熟悉常见实验用品是正确进行实验的基础.试回答以下问题:
化学是一门以实验为基础的科学,熟练使用中学化学实验中的常见仪器,熟悉常见实验用品是正确进行实验的基础.试回答以下问题:查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
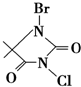 2013年夏季,南方个别城市遭到暴雨袭击,造成多人伤亡,暴雨过后,对环境进行消毒杀菌、获取洁净的饮用水都需要使用大量消毒剂,开发具有广谱、高效、低毒的杀菌、消毒剂非常重要.
2013年夏季,南方个别城市遭到暴雨袭击,造成多人伤亡,暴雨过后,对环境进行消毒杀菌、获取洁净的饮用水都需要使用大量消毒剂,开发具有广谱、高效、低毒的杀菌、消毒剂非常重要.查看答案和解析>>
科目: 来源: 题型:
| 加硫酸的次数序号 | 加入硫酸的体积/mL | 剩余固体的质量/g |
| 1 | 20.0 | 7.20 |
| 2 | 20.0 | 4.40 |
| 3 | 20.0 | 2.00 |
| 4 | 20.0 | 2.00 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 一定条件 |
| ||
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com