
科目: 来源: 题型:

| 实验 序号 | 0 | 10 | 20 | 30 | 40 | 50 | |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 950 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目: 来源: 题型:
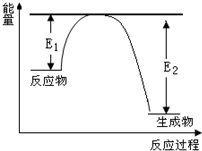 2013年12月2日我国成功发射的“嫦娥三号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:SiO2+C+N2
2013年12月2日我国成功发射的“嫦娥三号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:SiO2+C+N2| 高温 |
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
查看答案和解析>>
科目: 来源: 题型:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑨ | |||
| 4 | ② | ⑧ |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
c(N
| ||
| c(NH3?H2O) |
查看答案和解析>>
科目: 来源: 题型:
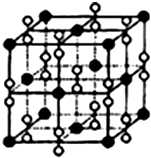 氧元素与多种元素具有亲和力,所形成化合物的种类仅次于碳元素.
氧元素与多种元素具有亲和力,所形成化合物的种类仅次于碳元素.查看答案和解析>>
科目: 来源: 题型:
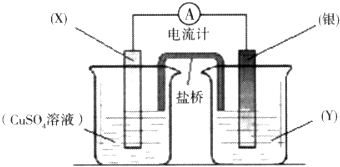
查看答案和解析>>
科目: 来源: 题型:
 物质的制备、分离、提纯、检验是化学实验中的重要内容,利用所学知识回答下列问题:
物质的制备、分离、提纯、检验是化学实验中的重要内容,利用所学知识回答下列问题:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com