
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 请写出图示燃料电池的反应式:
请写出图示燃料电池的反应式:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:


查看答案和解析>>
科目: 来源: 题型:
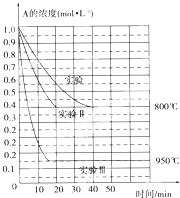 在一个体积为1L的密闭容器中发生某化学反应:2A(g)?B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在950℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示.试回答下列问题:
在一个体积为1L的密闭容器中发生某化学反应:2A(g)?B(g)+C(g),三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在950℃,B、C的起始浓度都为0,反应物A的浓度(mol?L-1)随时间(min)的变化如图所示.试回答下列问题:查看答案和解析>>
科目: 来源: 题型:
 工业上在合成塔中采用下列反应合成甲醇:
工业上在合成塔中采用下列反应合成甲醇:| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2molH2 | 1molCH3OH | 2molCH3OH | |
| 平衡 时数 据 | CH3OH的浓度(mol?L-1) | c1 | c2 | c3 |
| 反应吸收或放出的能量(KJ) | a | b | c | |
| 体系压强(Pa) | P1 | P2 | P3 | |
| 反应物转化率 | α1 | α2 | α3 | |
查看答案和解析>>
科目: 来源: 题型:
 某小组用0.10mo1?L-1 H2C204草酸溶液、0.01mol?L-1 KMn04溶液、O.10mol?L-1 H2S04溶液、一定量的蒸馏水等试剂,进行探究实验.
某小组用0.10mo1?L-1 H2C204草酸溶液、0.01mol?L-1 KMn04溶液、O.10mol?L-1 H2S04溶液、一定量的蒸馏水等试剂,进行探究实验.| 实验序号 | 体积V/mL | |||
| H2C204溶液 | 水 | KMn04溶液 | H2S04溶液 | |
| 1 | 10.O | 0.O | 4.O | 2.O |
| 2 | 8.O | 2.O | 4.O | 2.0 |
| 3 | 6.O | Vx | 4.O | 2.0 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com