
科目: 来源: 题型:
| 温度(℃) | 25 | 50 | 95 | |
| 溶解度(g) | 氯化钠 | 36.0 | 37.0 | 39.0 |
| 苯甲酸 | 0.17 | 0.95 | 6.8 | |
查看答案和解析>>
科目: 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ | |||||||
| 电离能I(eV) | A | B | C | D | E |
| I1 | 11.3 | 13.6 | 5.2 | 7.6 | 6.0 |
| I2 | 24.4 | 35.1 | 49.3 | 15.0 | 18.8 |
| I3 | 47.9 | 54.9 | 71.6 | 80.1 | 28.4 |
| I4 | 64.5 | 77.4 | 98.9 | 109.2 | 112.0 |
| I5 | 392.1 | 113.9 | 138.3 | 141.3 | 153.7 |
查看答案和解析>>
科目: 来源: 题型:
 (1)把除去氧化膜的铁丝投入到盛有稀硫酸的试管中,产生氢气的速率变化情况如图所示图中t1~t2速率变化的主要原因是
(1)把除去氧化膜的铁丝投入到盛有稀硫酸的试管中,产生氢气的速率变化情况如图所示图中t1~t2速率变化的主要原因是查看答案和解析>>
科目: 来源: 题型:
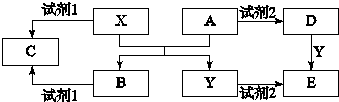
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
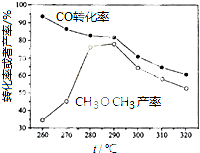 二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:查看答案和解析>>
科目: 来源: 题型:
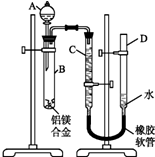 某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.
某学习小组用如图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com