
科目: 来源: 题型:
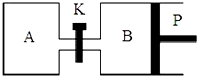 已知X(g)+Y(g)?2Z(g)+W(g)△H=-Q1kJ/mol(Q1>0),在一个有催化剂的固定容积的容器中加入1molX和1molY,在500℃时充分反应,达平衡后Z的浓度为w mol/L,放出热量Q2kJ.
已知X(g)+Y(g)?2Z(g)+W(g)△H=-Q1kJ/mol(Q1>0),在一个有催化剂的固定容积的容器中加入1molX和1molY,在500℃时充分反应,达平衡后Z的浓度为w mol/L,放出热量Q2kJ.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
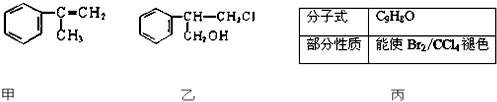
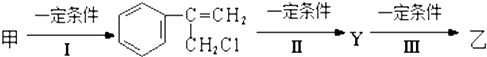
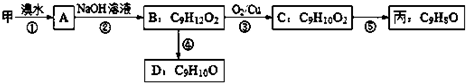
查看答案和解析>>
科目: 来源: 题型:
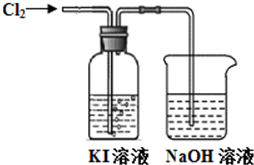 某同学对Cl2与KI溶液的反应进行了实验探究.反应装置如下:
某同学对Cl2与KI溶液的反应进行了实验探究.反应装置如下:| 操作 | 实验现象 | |
| a | 取2~3mL黄色溶液,加入足量CCl4,振荡静置. | CCl4层呈紫红色,水层显浅黄色. |
| b | 取2~3mL饱和碘水,加入足量CCl4,振荡静置. | CCl4层呈紫红色,水层几近无色. |
查看答案和解析>>
科目: 来源: 题型:
| c(NH4+) |
| c(NH3?H2O) |
| c(NH3?H2O) |
| c(OH-) |
| c(H+) |
| c(NH4+) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目: 来源: 题型:
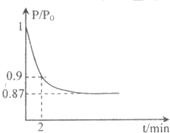 某实验小组模拟工业合成氨,利用合成的氨气验证氨气具有还原性实验.
某实验小组模拟工业合成氨,利用合成的氨气验证氨气具有还原性实验.| 催化剂 |
| 高温、高压 |
| P |
| P0 |
| 实验步骤 | 现象和结论 |
查看答案和解析>>
科目: 来源: 题型:
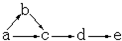 a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:
a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:查看答案和解析>>
科目: 来源: 题型:
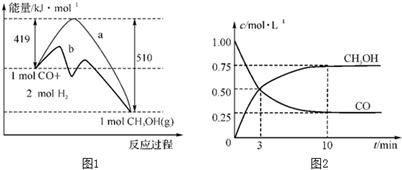
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com