(一) 尿素又称碳酰胺,是含氮量最高的氮肥,工业上利用二氧化碳和氨气在一定条件下合成尿素.其反应分为如下两步:
第一步:2NH
3(l)+CO
2(g)?H
2NCOONH
4(氨基甲酸铵)(l)△H
1=-330.0kJ?mol
-1第二步:H
2NCOONH
4(l)?H
2O(l)+H
2NCONH
2(l)△H
2=+226.3kJ?mol
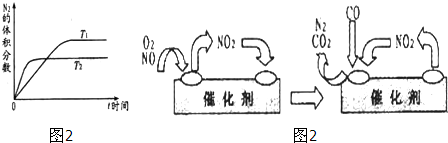
-1某实验小组模拟工业上合成尿素的条件,在一体积为0.5m
3密闭容器中投入4mol氨和1mol二氧化碳,实验测得反应中各组分的物质的量随时间的变化如图1所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第
步反应决定.
②反应进行到10min时测得CO
2的物质的量如图1所示,则用CO
2表示的第一步反应的速率v(CO
2)=
mol/(L?min).
③当反应在一定条件下达到平衡,若在恒温、恒容下再充入一定量气体He,则CO(NH
2)
2(l)的质量
(填“增加”、“减小”或“不变”).
(二)氨是制备尿素的原料,NH
3、N
2H
4等在工农业生产、航空航天等领域有广泛应用.
氨气溶于水得到氨水,在25℃下,将a mol/L的氨水与b mol/L的硫酸以3:2体积比混合反应后溶液呈中性.用含a和b的代数式表示出氨水的电离平衡常数为
.
(三)氢气是合成氨的原料.“氢能”将是未来最理想的新能源.
(1)在25℃,101KPa条件下,1g氢气完全燃烧生成液态水时放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为
.
(2)氢气通常用生产水煤气的方法制得.其中C(s)+H
2O(g)?CO(g)+H
2(g),在850℃时平衡常数K=1.若向1升的恒定密闭真空容器中同时加入x mol C和6.0mol H
2O.
①当加热到850℃反应达到平衡的标志有
.
A.容器内的压强不变 B.消耗水蒸气的物质的量与生成CO的物质的量相等
C.混合气的密度不变 D.单位时间有n个H-O键断裂的同时有n个H-H键断裂
②x应满足的条件是
.
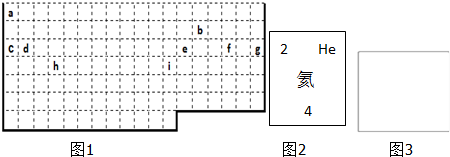
(四)CO
2是合成尿素的原料,但水泥厂生产时却排放出大量的CO
2.华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO
2零排放,其基本原理如图2所示:
(1)上述生产过程的能量转化方式是
.
(2)上述电解反应在温度小于900℃时进行碳酸钙先分解为CaO和CO
2,电解质为熔融碳酸钠,则阳极的电极反应式为
,阴极的电极反应式为
.

 B.
B. C.
C.
 E.
E. F.2-甲基丁烷和2,2-二甲基丙烷
F.2-甲基丁烷和2,2-二甲基丙烷