
科目: 来源: 题型:

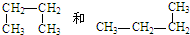 ⑧
⑧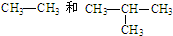
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 的沸点比
的沸点比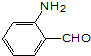 高,原因是
高,原因是查看答案和解析>>
科目: 来源: 题型:
| 实验方案 | 实验现象 |
| ①用砂纸打磨后的镁条与沸水反应,再向反应液中滴加酚酞 ②向新制的H2S饱和溶液中滴加新制的氯水(H2S是弱酸) ③钠与滴有酚酞试液的冷水反应 ④镁条与 ⑤铝条与 ⑥向AlCl3溶液中滴加NaOH溶液至过量 |
Ⅰ.浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红色 Ⅱ.放出无色气体,气体可燃,溶液变浅红色 Ⅲ.反应不十分强烈,产生的气体可燃 Ⅳ.剧烈反应,产生的气体可燃 Ⅴ.生成白色絮状沉淀,继而沉淀消失 Ⅵ.生成淡黄色沉淀 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com