
科目: 来源: 题型:
 ;⑥石墨;⑦14C;⑧CO2.
;⑥石墨;⑦14C;⑧CO2.查看答案和解析>>
科目: 来源: 题型:
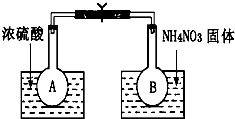 已知2NO2(g)?N2O4(g)△H=-52.7kJ?mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:
已知2NO2(g)?N2O4(g)△H=-52.7kJ?mol-1,某课外活动小组为了探究温度和压强对化学平衡的影响,做了如下两组实验:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
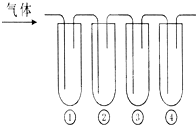 有一套实验装置,如图所示,可完成高中化学多种实验.装置①②③④中可以装试剂,也可用于气体的收集.
有一套实验装置,如图所示,可完成高中化学多种实验.装置①②③④中可以装试剂,也可用于气体的收集.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 实验步骤 | 实验现象 | 结论与化学方程式 |
| 三瓶溶液分别取样,分别加入x试剂.x试剂是 |
(1)有白色沉淀,加入过量x试剂,白色沉淀不消失; (2)先有白色沉淀,加入过量x试剂后,沉淀会消失; (3)无明显现象 |
该物质是 离子方程式是 该物质是 该物质是 |
查看答案和解析>>
科目: 来源: 题型:
| 催化剂 |
| 加热 |
| 温度℃ | 450 | 475 | 500 | 525 | 550 | 575 | 600 | 650 |
| SO2的转化率% | 97.5 | 95.8 | 95.8 | 93.5 | 90.50 | 85.6 | 80.0 | 73.7 |
查看答案和解析>>
科目: 来源: 题型:
| 燃烧 |
| MnO2 |
| △ |
| 强热 |
查看答案和解析>>
科目: 来源: 题型:

| 难溶 电解质 |
AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-12 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
查看答案和解析>>
科目: 来源: 题型:
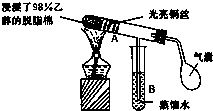 有关催化剂的催化机理等问题可从“乙醇催化氧化实验”得到一些认识,其实验装置如图所示:
有关催化剂的催化机理等问题可从“乙醇催化氧化实验”得到一些认识,其实验装置如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com