
科目: 来源: 题型:
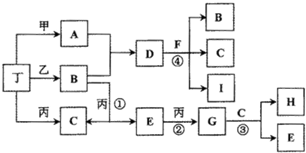
查看答案和解析>>
科目: 来源: 题型:
 某实验需要用1.0mol?L-1 NaOH 溶液500mL.
某实验需要用1.0mol?L-1 NaOH 溶液500mL.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 阳离子 | K+,Ba2+Fe2+Al3+ Fe3+ Mg2+ | ||||
| 阴离子 | OH-HCO
|
- 3 |
2- 3 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 ,每个COCl2分子内含有
,每个COCl2分子内含有
查看答案和解析>>
科目: 来源: 题型:
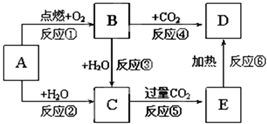 如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.它们的焰色反应均为黄色.请填写下列空白:
如图所示,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物.它们的焰色反应均为黄色.请填写下列空白:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com