
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 肼(N2H4)广泛用于火箭推进剂、有机合成及电池燃料.请回答下列问题:
肼(N2H4)广泛用于火箭推进剂、有机合成及电池燃料.请回答下列问题:| 实验Ⅰ:催化剂用量与配比对催化 活性影响 |
实验Ⅱ:水合肼用量对反应时间的影响 | 实验Ⅲ:反应温度对反应时间的影响 | ||||||||
| 序号 | m(Fe3+) /g |
m(Al3+) /g |
100%转化 消耗时间/min |
序号 | n(对氯硝基苯):n(水合肼) | 反应时间/min | 序号 | 反应温度/℃ | 反应时间/min | 转化率% |
| ① | 5 | 5 | 70 | ① | 1:1.5 | 110 | ① | 78 | 70 | 89 |
| ② | 10 | 不加 | 110 | ② | 1:1.8 | 110 | ② | 75 | 60 | 91 |
| ③ | 10 | 0.8 | 60 | ③ | 1:2.0 | 40 | ③ | 70 | 40 | 100 |
| ④ | 10 | 1 | 40 | ④ | 1:2.2 | 30 | ④ | 65 | 110 | 95 |
| ⑤ | 20 | 1 | 70 | / | / | / | ⑤ | 60 | 110 | 88 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
 某研究性学习小组欲探究“在加热条件下FeSO4的分解产物”?
某研究性学习小组欲探究“在加热条件下FeSO4的分解产物”?| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入 |
固体中含有Fe2O3 | |
| 向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液? | 产生蓝色沉淀 |
查看答案和解析>>
科目: 来源: 题型:
 现将0.40mol A气体和0.20mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量的变化如图:
现将0.40mol A气体和0.20mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量的变化如图:查看答案和解析>>
科目: 来源: 题型:
 纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:
纯铜在工业上主要用来制造导线、电器元件等,铜能形成+1和+2价的化合物.回答下列问题:查看答案和解析>>
科目: 来源: 题型:
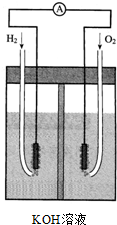 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com