
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
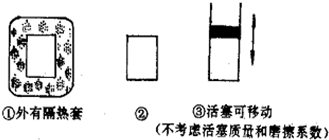
 如图所示,烧杯中都盛有稀硫酸.
如图所示,烧杯中都盛有稀硫酸.查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
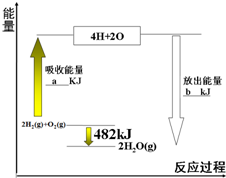 拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能.下表是某些共价键的键能:
拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能.下表是某些共价键的键能:| 共价键 | H-H | O=O | H-O |
| 键能/kJ?mol-1 | 436 | 498 | X |
查看答案和解析>>
科目: 来源: 题型:

| HBr |
| 催化剂 |
| 操作a |
| NaOH溶液 |
| △ |
| 操作B |
查看答案和解析>>
科目: 来源: 题型:
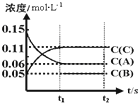 (1)在一个恒温恒容的密闭容器中,可逆反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡的标志是
(1)在一个恒温恒容的密闭容器中,可逆反应N2(g)+3H2(g)?2NH3(g)△H<0达到平衡的标志是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com