
科目: 来源: 题型:
| A、该粒子不显电性 |
| B、与氢元素的质子数相同 |
| C、该粒子质量数为4 |
| D、该粒子质量比氢原子大 |
查看答案和解析>>
科目: 来源: 题型:
| A、稳定性:H2O>H2S>H2Se |
| B、半径:Na+>Mg2+>F- |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目: 来源: 题型:
| A、气体分子的数目和分子本身的大小 |
| B、气体分子的质量和分子本身的大小 |
| C、气体分子的数目和分子间的平均距离 |
| D、气体分子本身的大小和分子间的平均距离 |
查看答案和解析>>
科目: 来源: 题型:
| A、O2是氧化剂,S2O32-和Fe2+是还原剂 |
| B、每生成1molFe3O4,则转移电子数为4mol |
| C、若有2molFe2+被氧化,则被Fe2+还原的O2为0.5mol |
| D、参加反应的氧化剂与还原剂的物质的最之比为1:5 |
查看答案和解析>>
科目: 来源: 题型:
| A、氢气是二次能源 |
| B、煤、石油、天然气均为化石能源 |
| C、只有农业废弃物、水生植物、油料植物中蕴含着丰富的生物质能 |
| D、太阳能是不可再生资源 |
查看答案和解析>>
科目: 来源: 题型:
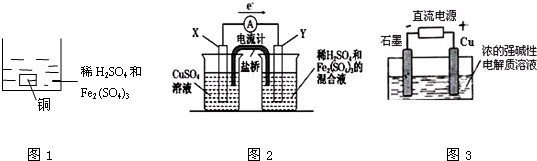
| A、如图1所示将一定量的铜片加入到100 mL稀硫酸和硫酸铁的混合溶液中,若铜片完全溶解时(不考虑盐的水解及溶液体积的变化),溶液中的Fe3+、Cu2+、H+三种离子的物质的量浓度相等,且测得溶液的pH=1,则溶液中c(SO42-)为0.5mol/L |
| B、如图2所示的装置中发生Cu+2Fe3+═Cu2++2Fe2+的反应,X极是负极,Y极的材料可以是铜 |
| C、Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图3所示,石墨电极上产生氢气,铜电极发生还原反应 |
| D、如图3所示,当有0.1mol电子转移时,有0.1mol Cu2O生成 |
查看答案和解析>>
科目: 来源: 题型:
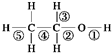
| A、乙醇和钠反应,键①断裂 |
| B、在Ag催化下和O2反应,键①③断裂 |
| C、乙醇和浓H2SO4共热140℃时,键①或键②断裂;在170℃时,键②⑤断裂 |
| D、乙醇完全燃烧时断裂键①② |
查看答案和解析>>
科目: 来源: 题型:
| A、①③⑤⑥ | B、③④⑤⑥ |
| C、②④⑤⑥ | D、①③④⑤ |
查看答案和解析>>
科目: 来源: 题型:
| A、①④⑥ | B、①②③④⑤ |
| C、①④ | D、①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com