
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).| 实验前 | 实验后 | |
| (干燥剂+U型管)的质量 | 101.1g | 113.7g |
| (石灰水+广口瓶)的质量 | 312.0g | 338.4g |
查看答案和解析>>
科目: 来源: 题型:
| ① | ||||||||
| ② | ③ | ④ | ||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||||
查看答案和解析>>
科目: 来源: 题型:
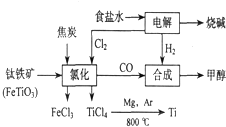 钛(Ti)被称为继铁、铝之后的第三金属.如图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染.请填写下列空白:
钛(Ti)被称为继铁、铝之后的第三金属.如图所示,将钛厂、氯碱厂和甲醇厂组成产业链可以大大提高资源利用率,减少环境污染.请填写下列空白:查看答案和解析>>
科目: 来源: 题型:
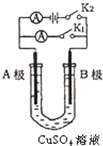 如图所示,U形管内盛有100mL的CuSO4溶液,按要求回答下列问题:
如图所示,U形管内盛有100mL的CuSO4溶液,按要求回答下列问题:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目: 来源: 题型:
| 化学键 | Si-O | O═O | Si-Si |
| 键能/kJ?mol-1 | x | 498.8 | 176 |
查看答案和解析>>
科目: 来源: 题型:
| 一定含有的离子种类 | |||||||
| 物质的量浓度(mol/L) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com