
科目: 来源: 题型:
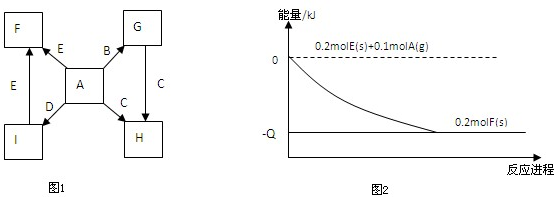
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
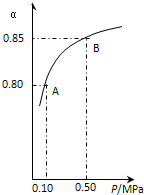 二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.| 催化剂 |
| △ |
查看答案和解析>>
科目: 来源: 题型:
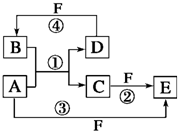 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).查看答案和解析>>
科目: 来源: 题型:
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | ⅦA | |
| 2 | ⑩ | ② | ③ | ④ | ⑧ | |||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ||||
查看答案和解析>>
科目: 来源: 题型:
 |
ⅠA |
ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | K | G | ||||
| 3 | B | C | J | F | H | I |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
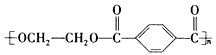 .现以煤的干馏产品A与F为原料制备PET,生产流程如图所示.其中A为烃,含碳元素的质量分数为90.6%,其蒸气的密度是空气密度的3.66倍,能使酸性高锰酸钾溶液褪色,但不能使溴水褪色.M分子里所有原子共平面.
.现以煤的干馏产品A与F为原料制备PET,生产流程如图所示.其中A为烃,含碳元素的质量分数为90.6%,其蒸气的密度是空气密度的3.66倍,能使酸性高锰酸钾溶液褪色,但不能使溴水褪色.M分子里所有原子共平面.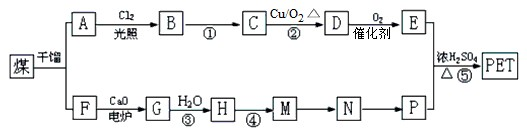
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com