
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 如图所示为电解水的装置,闭合开关s后,观察到电压表示数为6.0V,电流表示数为100mA.
如图所示为电解水的装置,闭合开关s后,观察到电压表示数为6.0V,电流表示数为100mA.查看答案和解析>>
科目: 来源: 题型:
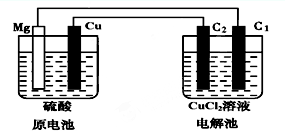 某研究性学习小组的课题为“Mg-Cu硫酸原电池电解CuCl2溶液的研究”,他们的研究装置如图所示(C1、C2均为碳棒),按要求填写下列空格.
某研究性学习小组的课题为“Mg-Cu硫酸原电池电解CuCl2溶液的研究”,他们的研究装置如图所示(C1、C2均为碳棒),按要求填写下列空格.查看答案和解析>>
科目: 来源: 题型:
 下列化合物:①HCl ②NaOH ③CH3COOH ④NH3?H2O ⑤CH3COONa ⑥NH4Cl ⑦C2H5OH ⑧SO2
下列化合物:①HCl ②NaOH ③CH3COOH ④NH3?H2O ⑤CH3COONa ⑥NH4Cl ⑦C2H5OH ⑧SO2查看答案和解析>>
科目: 来源: 题型:
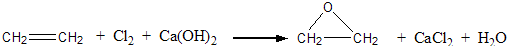
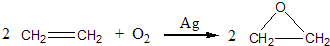
查看答案和解析>>
科目: 来源: 题型:
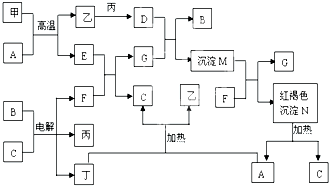 如图为中学常见物质间的转化关系,其中甲、乙、丙、丁为单质,其余为化合物,甲单质所含元素最外层电子数等于周期数,C常温下为无色液体,B焰色反应为黄色.一些在溶液中进行的反应溶液中的H2O及生成的H2O已省略.回答下列问题:
如图为中学常见物质间的转化关系,其中甲、乙、丙、丁为单质,其余为化合物,甲单质所含元素最外层电子数等于周期数,C常温下为无色液体,B焰色反应为黄色.一些在溶液中进行的反应溶液中的H2O及生成的H2O已省略.回答下列问题:查看答案和解析>>
科目: 来源: 题型:
 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用如图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用如图装置完成了O元素的非金属性比S强的实验研究.回答下列问题:查看答案和解析>>
科目: 来源: 题型:
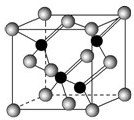 Ⅰ.2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED).目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.已知镓是铝同族下一周期的元素.砷化镓的晶胞结构如右图所示.试回答:
Ⅰ.2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED).目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.已知镓是铝同族下一周期的元素.砷化镓的晶胞结构如右图所示.试回答:查看答案和解析>>
科目: 来源: 题型:
 (1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
(1)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com