
科目: 来源: 题型:
| A、向Mg(OH)2悬浊液中加入FeCl3溶液:3OH-+Fe3+═Fe(OH)3↓ |
| B、淀粉碘化钾溶液在空气中变蓝:4I-+O2+2H2O=4OH-+2I2 |
| C、用酸性K2Cr2O7溶液检验酒精:3CH3CH2OH+2Cr2O72-+13H+=4Cr3++11H2O+3CH3COO- |
| D、次氯酸钠溶液中通入二氧化硫气体:2ClO-+SO2+H2O═2HClO+SO32- |
查看答案和解析>>
科目: 来源: 题型:
| A、汽车尾气中的氮氧化物与光化学烟雾形成有关 |
| B、电解氯化铝溶液可获得金属铝 |
| C、大量燃烧含硫燃料是形成酸雨的主要原因 |
| D、铜具有良好的导电性,常用来制作印刷电路板 |
查看答案和解析>>
科目: 来源: 题型:
| 试管 | 盐酸浓度 | 温度 | 锌的状态 |
| A | 0.5mol?L-1 | 30℃ | 块 状 |
| B | 0.5mol?L-1 | 30℃ | 粉末状 |
| C | 1mol?L-1 | 35℃ | 块 状 |
| D | 1mol?L-1 | 35℃ | 粉末状 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目: 来源: 题型:
| A、医疗上的血液透析利用了胶体的性质,而土壤保肥与胶体的性质无关 |
| B、蔗糖、淀粉、油脂及其水解产物均为非电解质 |
| C、通过红外光谱分析可以区分乙醇和乙酸乙酯 |
| D、乙醇、乙酸均能与Na反应放出H2,二者分子中官能团种类相同 |
查看答案和解析>>
科目: 来源: 题型:
 如图装置中发生反应的离子方程式为:Cu+2H+=Cu2++H2↑,下列说法正确的是( )
如图装置中发生反应的离子方程式为:Cu+2H+=Cu2++H2↑,下列说法正确的是( )| A、a、b不可能是同种材料的电极 |
| B、该装置可能是原电池,电解质溶液为稀盐酸 |
| C、该装置可能是a、b未形成闭合回路,电解质溶液是稀硝酸 |
| D、该装置可能是电解池,电解质溶液为稀盐酸 |
查看答案和解析>>
科目: 来源: 题型:
 常温下将HA和HB两种一元酸的溶液分别加水稀释,稀释时溶液pH的变化如图所示.以下叙述中不正确的是.( )
常温下将HA和HB两种一元酸的溶液分别加水稀释,稀释时溶液pH的变化如图所示.以下叙述中不正确的是.( )| A、HB是一种弱酸 |
| B、稀释前,c(HA)<10c(HB) |
| C、在NaB和HB的混合溶液中一定存在:c(B-)>c(Na+)>c(H+)>c(OH-) |
| D、在M点的两种溶液中:c(B-)=c(A-),且c(B-)+c(H+)>c(A-)+c(OH-) |
查看答案和解析>>
科目: 来源: 题型:
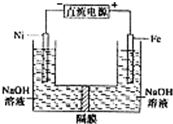 高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示.下列推断合理的是( )| A、铁是阳极,电极反应为Fe-6e-+4H2O═FeO42-+8H |
| B、电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 |
| C、若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D、电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
查看答案和解析>>
科目: 来源: 题型:
| A、该电池替代现在电动车广泛使用的铅蓄电池可以减少重金属的污染 |
| B、该电池放电时溶液中Li+的离子移向正极 |
| C、该电池的负极电极反应式为Al-3e-=Al3+ |
| D、充电时,阴极发生的电极反应式为Li2S+Fe-2e-=2Li++FeS |
查看答案和解析>>
科目: 来源: 题型:
| A、该反应中H2O是反应物之一 |
| B、氧化剂与还原剂的物质的量之比为1:5 |
| C、氧化产物为HIO3 |
| D、若有1mol I2参加氧化反应,转移10mol e- |
查看答案和解析>>
科目: 来源: 题型:
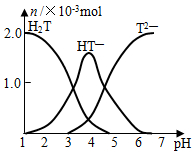 常温下,向20mL 0.1mol/L酒石酸(用H2T表示)溶液中逐滴滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系.下列说法正确的是( )
常温下,向20mL 0.1mol/L酒石酸(用H2T表示)溶液中逐滴滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系.下列说法正确的是( )| A、VNaOH=10mL时,溶液中存在[Na+]=2[H2T]+2[HT-]+2[T2-] |
| B、VNaOH=20mL时,溶液中存在[Na+]>[HT-]>[H+]>[H2T]>[T2-] |
| C、VNaOH=30mL时,溶液中存在[Na+]>[HT-]>[T2-]>[OH-]>[H+] |
| D、VNaOH=40mL时,溶液中存在[OH-]=[HT-]+2[H2T]+[H+] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com