
科目: 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 容器 | A | B |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| 反应能量变化 | 放出αkJ热量 | 吸收19.6kJ热量 |
查看答案和解析>>
科目: 来源: 题型:

| 棉球 | 棉球上滴加的试剂 | 实验现象 | 解释和结论 |
| a | 棉球变白,微热后又恢复红色 | ||
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: |
| c | 棉球变为白色 | 结论:该气体具有 |
查看答案和解析>>
科目: 来源: 题型:
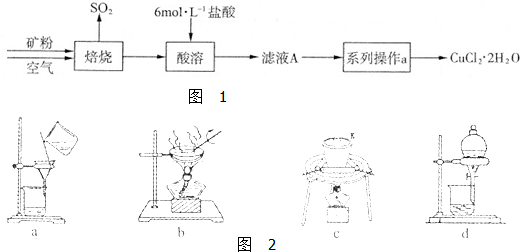

| ① |
| ② |
| ③ |
| ④ |

查看答案和解析>>
科目: 来源: 题型:
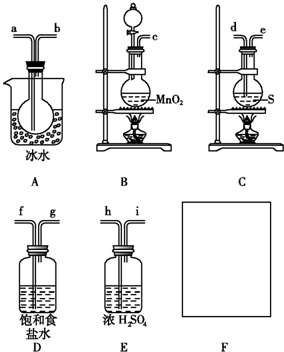 S2Cl2常用于橡胶硫化,有机物氯化的试剂,某研究性学习小组拟用实验室常用试剂和仪器合成S2Cl2.
S2Cl2常用于橡胶硫化,有机物氯化的试剂,某研究性学习小组拟用实验室常用试剂和仪器合成S2Cl2.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
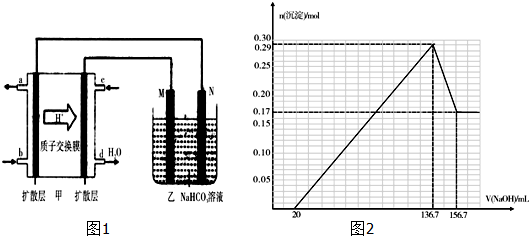
查看答案和解析>>
科目: 来源: 题型:
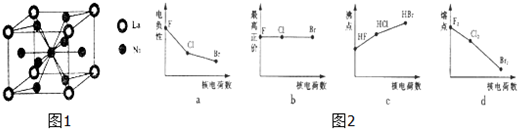
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com