
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
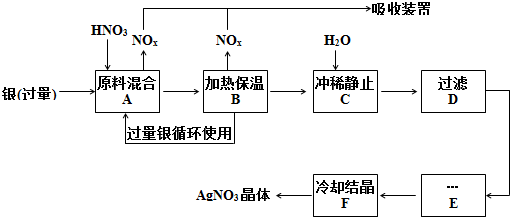
| 优点 | 缺点 | |
| 使用浓硝酸 | 反应速率快 | 酸耗较大,产生NOx的量较多 |
| 使用稀硝酸 |
查看答案和解析>>
科目: 来源: 题型:
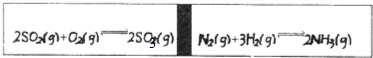 在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)
在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)查看答案和解析>>
科目: 来源: 题型:
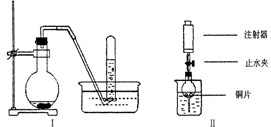 某同学甲采用如下图I所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体.
某同学甲采用如下图I所示装置验证铜与稀硝酸的反应,并用排水法收集NO气体.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 2 | 3 | 0 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com