
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
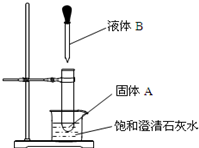 如图所示,把试管放入盛有25℃的饱和石灰水溶液的烧杯中,试管中开始放入固体试剂A,再用再用滴定管滴入5mL液体试剂B于试管中.可见到烧杯中饱和石灰水变浑浊.试回答下列问题:
如图所示,把试管放入盛有25℃的饱和石灰水溶液的烧杯中,试管中开始放入固体试剂A,再用再用滴定管滴入5mL液体试剂B于试管中.可见到烧杯中饱和石灰水变浑浊.试回答下列问题:查看答案和解析>>
科目: 来源: 题型:
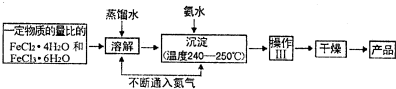
| 步骤 | 实验操作 | 实验现象、结论 |
| 1 | 取一定量3mol/L硫酸溶液于试管中,加热煮沸去除溶解氯气 | / |
| 2 | 取少量产品于试管中,加适量步骤1处理好的溶液,溶解、配成溶液 | 固体溶解,溶液呈浅黄色 |
| 3 | 取少量步骤2配好的溶液于试管中,滴加几滴20%硫氰化钾溶液,振荡 | |
| 4 | |
| 1 |
| 10 |
查看答案和解析>>
科目: 来源: 题型:
 如图是某医院输液用的一瓶葡萄糖注射液标签的部分内容.据此回答以下问题(答案保留2位小数):
如图是某医院输液用的一瓶葡萄糖注射液标签的部分内容.据此回答以下问题(答案保留2位小数):查看答案和解析>>
科目: 来源: 题型:
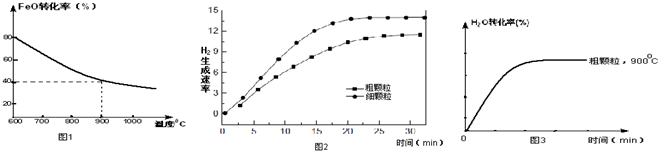
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
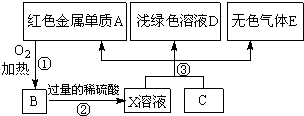 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com