
科目: 来源: 题型:
| 盐酸 |
| NaOH溶液 |
| 盐酸 |
| 适量NaOH溶液 |
查看答案和解析>>
科目: 来源: 题型:
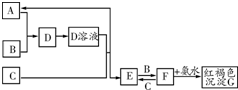 如图中A、B为常见气体单质,B为黄绿色气体,C为生活中常见金属.请按要求填空:
如图中A、B为常见气体单质,B为黄绿色气体,C为生活中常见金属.请按要求填空:查看答案和解析>>
科目: 来源: 题型:
 元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.
元素在周期表中的位置,反映了元素的原子结构和元素的性质.如图是元素周期表的一部分.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 糖类、脂肪、蛋白质、维生素、矿物质(无机盐)和水合称六大营养素,食物烹调时还使用一些调味剂.张华家今晚菜谱如图.
糖类、脂肪、蛋白质、维生素、矿物质(无机盐)和水合称六大营养素,食物烹调时还使用一些调味剂.张华家今晚菜谱如图.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com