
科目: 来源: 题型:
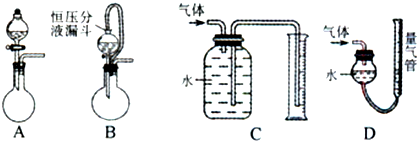
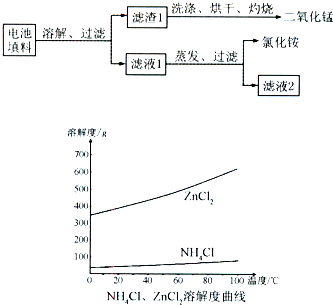
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
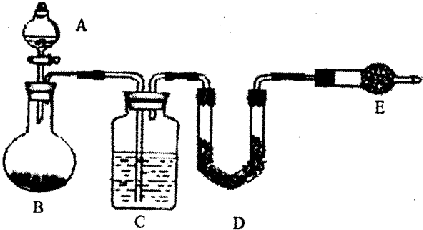 某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数.
某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 Ⅰ.(1)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液中c(Na+)
Ⅰ.(1)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液中c(Na+)查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 ③
③ ④
④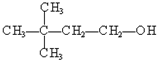 ⑤
⑤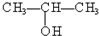
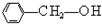 )
)查看答案和解析>>
科目: 来源: 题型:
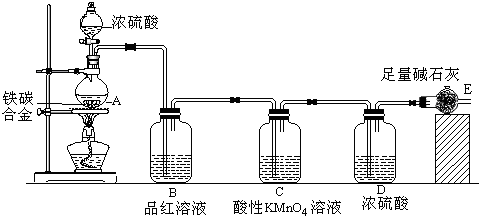
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com