
科目: 来源: 题型:

| 测试时间(h) | 0 | 1 | 2 | 4 | 8 |
| 雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
查看答案和解析>>
科目: 来源: 题型:
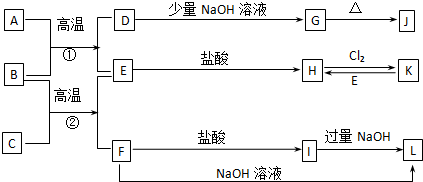
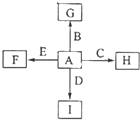 如图中,A为空气中常见的气体单质、B、C、E是金属单质,D为非金属单质.已知:①I是一种常见的温室气体,E原子核内有12个质子②G是一种红棕色固体粉末,反应C+G
如图中,A为空气中常见的气体单质、B、C、E是金属单质,D为非金属单质.已知:①I是一种常见的温室气体,E原子核内有12个质子②G是一种红棕色固体粉末,反应C+G| 高温 |
| 高温 |
| ||
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| ①分别取等体积的2mol.L-1 H2SO4 于试管中 ②分别投入大小、形状相同的 Cu、Fe、 Mg. |
镁反应速率比铁快, 铜不反应 |
(1) |
 (3)用此装置进行定量实验,应选用上述的实验药品是:
(3)用此装置进行定量实验,应选用上述的实验药品是:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
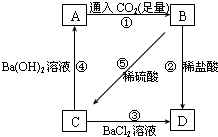 现有A、B、C、D四种溶液,在进行焰色反应时,火焰颜色都为黄色,它们之间转化关系如图所示.已知B为NaHCO3,请回答下列问题:
现有A、B、C、D四种溶液,在进行焰色反应时,火焰颜色都为黄色,它们之间转化关系如图所示.已知B为NaHCO3,请回答下列问题:查看答案和解析>>
科目: 来源: 题型:
 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com