
科目: 来源: 题型:
 工业上可用煤制天然气,生产过程中有多种途径生成CH4.
工业上可用煤制天然气,生产过程中有多种途径生成CH4.查看答案和解析>>
科目: 来源: 题型:
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.| 催化剂 |
| 加热 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
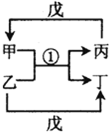 A~H均为短周期元素,A~F在元素周期表中的相对位置如表所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素.由B、G构成的最简单化合物常为氮肥工业和纯碱工业的原料.由上述某些元素组成的物质甲~戊的转化关系如图所示.请回答下列问题:
A~H均为短周期元素,A~F在元素周期表中的相对位置如表所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素.由B、G构成的最简单化合物常为氮肥工业和纯碱工业的原料.由上述某些元素组成的物质甲~戊的转化关系如图所示.请回答下列问题:| A | B | C | |
| D | E | F |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
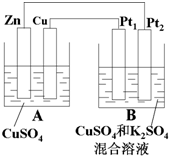 如图A、B两个装置,回答下列问题:
如图A、B两个装置,回答下列问题:查看答案和解析>>
科目: 来源: 题型:
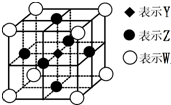 已知:X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大.X的简单阴离子最外层有2个电子,Y原子最外层电子数是内层电子数的两倍,Z的原子序数是Y的两倍,在元素周期表中W元素位于第11列.
已知:X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大.X的简单阴离子最外层有2个电子,Y原子最外层电子数是内层电子数的两倍,Z的原子序数是Y的两倍,在元素周期表中W元素位于第11列.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com