
科目: 来源: 题型:
| A | B | C | D | |
| SO3 | 0mol | 4mol | 2mol | 0mol |
| SO2 | 4mol | 1.5mol | 0mol | 4mol |
| O2 | 2mol | 0mol | 0mol | 4mol |
查看答案和解析>>
科目: 来源: 题型:
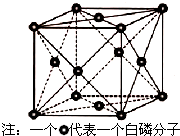 VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题.
VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题.查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| 高温高压 |
| 催化剂 |
| 时间/h 物质的量/mol |
0 | 1 | 2 | 3 | 4 |
| N2 | 2.0 | 1.83 | 1.7 | 1.6 | 1.6 |
| H2 | 6.0 | 5.49 | 5.1 | 4.8 | 4.8 |
| NH3 | 0 | 0.34 | 0.6 | 0.8 | 0.8 |
| 一定条件 |
| 通电 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:


| NH3?H2O | Kb=1.8×10-5mol?L-1 |
| H2SO3 | Ka1=1.2×10-2mol?L-1 Ka2=1.3×10-8mol?L-1 |
查看答案和解析>>
科目: 来源: 题型:
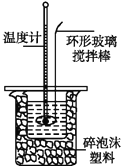 依据叙述,写出下列反应的热化学方程式.
依据叙述,写出下列反应的热化学方程式.查看答案和解析>>
科目: 来源: 题型:
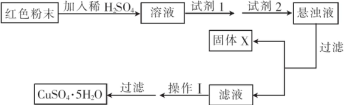
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时的pH | 6.0 | 7.5 | 1.4 |
| 完全沉淀时的pH | 13 | 14 | 3.7 |
查看答案和解析>>
科目: 来源: 题型:
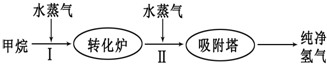
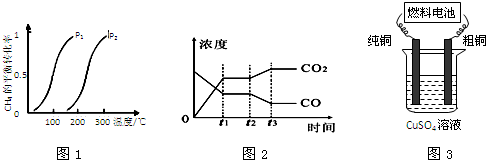
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
查看答案和解析>>
科目: 来源: 题型:
| 序号 | 物质 | 除杂试剂 |
| (1) | CO2(HCl) | |
| (2) | Fe2O3(Al2O3) | |
| (3) | NaCl溶液(MgCl2) | |
| (4) | NO气体(NO2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com