
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
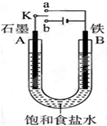 某课外活动小组同学用如图装置进行实验,试回答下列问题.
某课外活动小组同学用如图装置进行实验,试回答下列问题.查看答案和解析>>
科目: 来源: 题型:
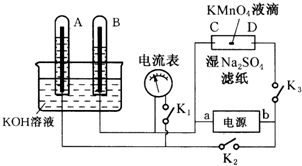 A、B为充满KOH溶液的两只试管.切断K1,合闭K2、K3,通直流电,电解一段时间后A、B中均有气体产生.装置如图.回答下列问题:
A、B为充满KOH溶液的两只试管.切断K1,合闭K2、K3,通直流电,电解一段时间后A、B中均有气体产生.装置如图.回答下列问题:查看答案和解析>>
科目: 来源: 题型:
| 元素 | 性质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物可发生非氧化还原反应 |
| D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
| E | 在地壳中的含量位居第三 |
| F | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| G | 该元素的一种氧化物M可用作油漆颜料,与E的单质反应可应用于焊接钢轨 |
查看答案和解析>>
科目: 来源: 题型:
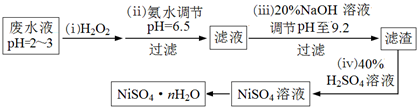
查看答案和解析>>
科目: 来源: 题型:
 某校环保小组处理污水样品,需要配制500mL0.1mol/L的硫酸溶液.
某校环保小组处理污水样品,需要配制500mL0.1mol/L的硫酸溶液.查看答案和解析>>
科目: 来源: 题型:
| A、c(HCN)>c(CN-) |
| B、c(Na+)>c(CN-) |
| C、c(HCN)-c(CN-)=c(OH-) |
| D、c(HCN)+c(CN-)=0.1mol/L |
查看答案和解析>>
科目: 来源: 题型:

| A、在外电路中,电子由银电极流向铜电极 |
| B、正极反应为:Ag++e-=Ag |
| C、实验过程中取出盐桥,原电池仍能继续工作 |
| D、盐桥中的K+移向Cu(NO3)2溶液 |
查看答案和解析>>
科目: 来源: 题型:
| A、标准状况下,44.8L NO与22.4L O2混合气体中分子总数等于3NA |
| B、已知2CO(g)+O2(g)?2CO2(g)△H=-a kJ?mol-1将2NA个CO与NA个O2混合充分反应放出akJ的热量 |
| C、50mL 18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D、2.3g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA |
查看答案和解析>>
科目: 来源: 题型:
| A、(NH4)2SO4溶液中c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| B、Na2S稀溶液中c(Na+)=c(S2-)+c(H2S)+c(HS-) |
| C、饱和食盐水中c(Na+)+c(H+)=c(Cl-)+c(OH-) |
| D、CH3COOH溶液加水稀释后,溶液中所有离子浓度都减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com