
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 放电 |
| 充电 |
查看答案和解析>>
科目: 来源: 题型:
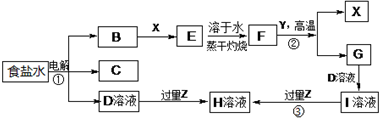
 电解原理在化学工业中有广泛的应用.图1表示一个电解池,
电解原理在化学工业中有广泛的应用.图1表示一个电解池,查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
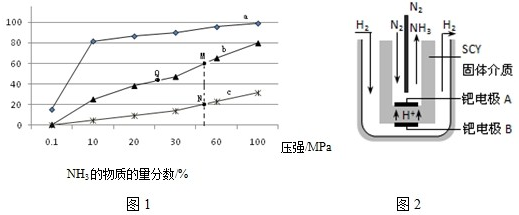
| 436.0kJ?mol-1 |
| 945.8kJ?mol-1 |
查看答案和解析>>
科目: 来源: 题型:
 莽草酸可从八角中提取,它是制取抗甲型H1N1流感药物(达菲)的原料.莽草酸的结构式如图.请回答以下问题:
莽草酸可从八角中提取,它是制取抗甲型H1N1流感药物(达菲)的原料.莽草酸的结构式如图.请回答以下问题:查看答案和解析>>
科目: 来源: 题型:
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ?mol-1 | 436 | a | 945 |

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
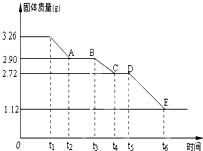 (1)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A.根据题意回答下列问题:
(1)常温下,某水溶液M中存在的离子有:Na+、A2-、HA-、H+、OH-,存在的分子有H2O、H2A.根据题意回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com