
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 丙烯醛(结构简式:CH2=CHCHO)是一种重要的有机合成原料,外观为无
丙烯醛(结构简式:CH2=CHCHO)是一种重要的有机合成原料,外观为无查看答案和解析>>
科目: 来源: 题型:
| 活性炭/mol | NO/mol | A/mol | B/mol | |
| 起始状态 | 2.030 | 0.100 | 0 | 0 |
| 2min时 | 2.000 | 0.040 | 0.030 | 0.030 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
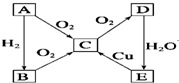 已知,A为空气中含量最多的单质.根据如下图转化关系,回答下列问题:
已知,A为空气中含量最多的单质.根据如下图转化关系,回答下列问题:查看答案和解析>>
科目: 来源: 题型:
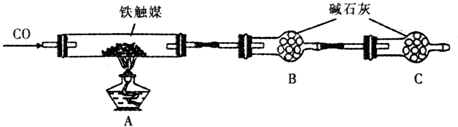
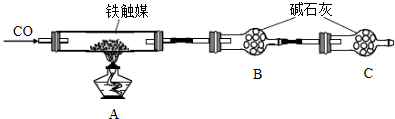
 如右图所示,某气体X可能由H2、CO、CH4中的一种或几种组成.将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶.
如右图所示,某气体X可能由H2、CO、CH4中的一种或几种组成.将X气体燃烧,把燃烧后生成的气体通过A、B两个洗气瓶.查看答案和解析>>
科目: 来源: 题型:
| c(H+) |
| c(OH-) |
| c(H+) |
| c(H2C2O4) |
c(C2
| ||
c(HC2
|
c2(H+)?c(C2
| ||
| c(H2C2O4) |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| 实验操作 | 实验现象与结论 |
| 取适量溶液B于试管中,滴加 ,放置一段时间后,观察现象. |
若溶液 若溶液 |
查看答案和解析>>
科目: 来源: 题型:

| 实验操作 | 实验现象与结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com