
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 把18.0mol/L 的浓硫酸稀释成1.80mol/L 的稀硫酸100mL,实验操作如下:
把18.0mol/L 的浓硫酸稀释成1.80mol/L 的稀硫酸100mL,实验操作如下:查看答案和解析>>
科目: 来源: 题型:
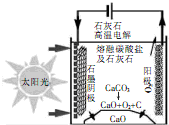 资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.
资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
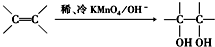 .请写出有机化合物A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式:
.请写出有机化合物A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
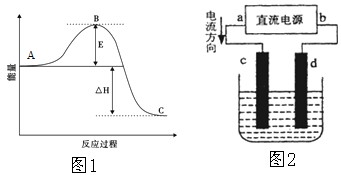
| 7 |
| 10 |
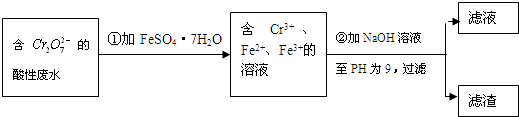
查看答案和解析>>
科目: 来源: 题型:
 和
和 D.35Cl和37Cl E.乙醇和乙二醇
D.35Cl和37Cl E.乙醇和乙二醇查看答案和解析>>
科目: 来源: 题型:
A、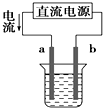 如图装置中a为阳极、b为阴极 |
B、 如图装置的总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
C、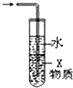 如图装置中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
D、 如图装置中的铁钉几乎不被腐蚀 |
查看答案和解析>>
科目: 来源: 题型:
| A、向溶液中加入少量KCl晶体 |
| B、向溶液中加入一定量KCl溶液 |
| C、向溶液中加少量AgNO3固体 |
| D、向溶液中滴加几滴1 mol?L-1FeCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com