
科目: 来源: 题型:
| A、CH3CH2OH(l)+3O2 (g)=2CO2 (g)+3H2O(l)△H=-a kJ/mol | ||
| B、CH4 (g)+2O2 (g)=2H2O(g)+CO2(g)△H=-b kJ/mol | ||
C、H2 (g)+
| ||
| D、2CH≡CH(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-d kJ/mol |
查看答案和解析>>
科目: 来源: 题型:
 O3可通过臭氧发生器电解稀硫酸制得(原理如图).下列有关说法不正确的是( )
O3可通过臭氧发生器电解稀硫酸制得(原理如图).下列有关说法不正确的是( )| A、电极A为阴极 |
| B、质子由A极通过交换膜移向B极 |
| C、若C极通入O2,则A的电极反应式为O2+4e-+4H+═2H2O |
| D、若C处不通入O2,D、E处分别收集到15.68L和6.72L气体(标准状况),则E处收集的气体中O2和O3的体积比为2:1(忽略O3的分解) |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
- 2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
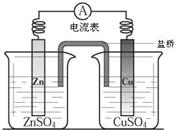 原电池是化学电池的雏形.如图是一次性电池--铜锌电池的简易装置.
原电池是化学电池的雏形.如图是一次性电池--铜锌电池的简易装置.查看答案和解析>>
科目: 来源: 题型:
 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如右下图所示装置.试回答下列问题:
将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如右下图所示装置.试回答下列问题:查看答案和解析>>
科目: 来源: 题型:
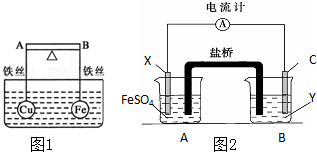 (1)如图1所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中央滴入浓硫酸铜溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)当杠杆为绝缘体时,A端比B端
(1)如图1所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中央滴入浓硫酸铜溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)当杠杆为绝缘体时,A端比B端查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com