
科目: 来源: 题型:
| A、在常温常压下,14g N2含有的分子数为0.5NA |
| B、25℃、101.3kPa时,11.2LH2中含有的原子数为NA |
| C、标准状况下,1mol CCl4的体积约为22.4L |
| D、2.3g的金属钠变为钠离子时失去的电子数为0.2NA |
查看答案和解析>>
科目: 来源: 题型:
| A、此时,B的平衡转化率是40% | ||
| B、增加B,平衡向右移动,B的平衡转化率增大 | ||
C、该反应的化学平衡常数表达式是K=
| ||
| D、增大该体系的压强,平衡向右移动,化学平衡常数增大 |
查看答案和解析>>
科目: 来源: 题型:
| A、二氧化硫使溴水褪色 SO2+Br2+2H2O=4H++SO42-+2Br- |
| B、用食醋清洗热水瓶胆内壁附着的水垢(CaCO3) CO32-+2H+=CO2↑+H2O |
| C、硫酸铜与Ba(OH)2溶液反应 Cu2++2OH-=Cu(OH)2↓ |
| D、少量CO2通入Na2SiO3溶液:CO2+SiO32-+H2O=CO32-+H2SiO3↓ |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 3 |
| 2 |
| 3 |
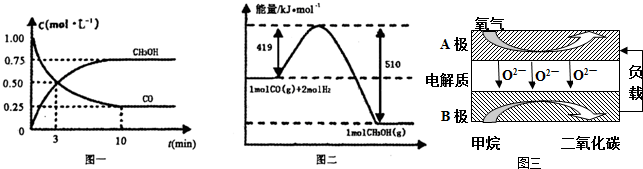
| 容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化(Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| ①H2SO4溶液中H2SO4 | ①H2SO4溶液中HSO4- | ②NaHSO4溶液中HSO4- | ③CH3COOH 溶液 |
④HCl溶液 |
| 100% | 10% | 29% | 1.3% | 100% |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com