
科目: 来源: 题型:
 的化合物称为二肽,二肽还可以继续与其它α-氨基酸分子脱水形成三肽、四肽以至生成长链的多肽.若丙氨酸[CH3CH(NH2)COOH]与甘氨酸[H2N-CH2-COOH]的混合物在一定条件下反应,可形成
的化合物称为二肽,二肽还可以继续与其它α-氨基酸分子脱水形成三肽、四肽以至生成长链的多肽.若丙氨酸[CH3CH(NH2)COOH]与甘氨酸[H2N-CH2-COOH]的混合物在一定条件下反应,可形成查看答案和解析>>
科目: 来源: 题型:
| 编号 | A | B | C | D | E | F | G | H |
| 物质 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
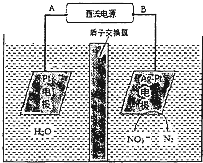 化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.
化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.查看答案和解析>>
科目: 来源: 题型:
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4mL 2mol?L-1 HCl溶液 | 沉淀溶解 |
| Ⅱ | 4mL 2mol?L-1 NH4Cl溶液 | 沉淀溶解 |
查看答案和解析>>
科目: 来源: 题型:
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,测定溶液pH | pH=0 |
| (2)取少量该溶液加热浓缩,加Cu片和浓 H2SO4,加热 | 有无色气体产生,气体遇空气变成红棕色 |
| (3)取少量该溶液,加少量BaCl2溶液 | 有白色沉淀 |
| (4)取(3)中上层清液,加足量AgNO3溶液 | 有白色沉淀,且不溶于稀HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀,NaOH过量时沉淀部分溶解 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
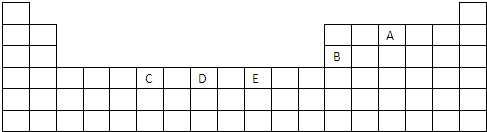
| Na | Mg | Si | |
| I1/kJ?mol-1 | 496 | 738 | 787 |
查看答案和解析>>
科目: 来源: 题型:
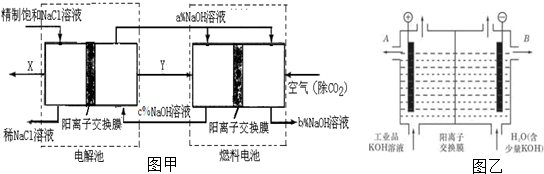
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com