
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 族元素;E和C位于同一主族,F的原子序数为24.
族元素;E和C位于同一主族,F的原子序数为24.查看答案和解析>>
科目: 来源: 题型:
| 2 |
| 3 |
查看答案和解析>>
科目: 来源: 题型:
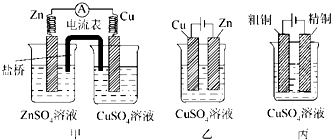
查看答案和解析>>
科目: 来源: 题型:
 下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: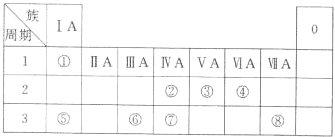
| 编号 | 性质 | 化学方程式或文字说明 |
| 示例 | 漂白性 | 与某些有色物质形成不稳定的无色物质 |
| Ⅰ | 还原性 | 2H2O+2SO2+O2=2HSO4 |
| Ⅱ | ||
| Ⅲ |
查看答案和解析>>
科目: 来源: 题型:
| 时间t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCL3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 利用如图所示装置测定中和热的实验步骤如下:
利用如图所示装置测定中和热的实验步骤如下:查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| O2 |
| △ |
| 盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com