
科目: 来源: 题型:
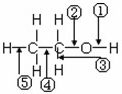
| 反应 | 断键 | 对应的化学方程式 |
| 乙醇和钠的反应 | ||
| 乙醇和乙酸浓硫酸共热 | ||
| 在银催化下和氧气作用 |
查看答案和解析>>
科目: 来源: 题型:
| H+ |
| ①转化 |
2- 7 |
| Fe+ |
| ②还原 |
| OH- |
| ③沉淀 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 实验编号 | 待测血液的体积/mL | 滴入KMnO4溶液的体积/mL |
| 1 | 20.00 | 11.95 |
| 2 | 20.00 | 13.00 |
| 3 | 20.00 | 12.05 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 0.01mol/L的溶液 | X | Y | Z | W |
| PH | 12 | 2 | 8.5 | 4.5 |
查看答案和解析>>
科目: 来源: 题型:
A、聚丙烯酸钠的结构式为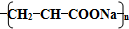 |
| B、聚丙烯酸钠可以通过单体发生缩聚反应制得 |
| C、聚丙烯酸钠具有热塑性 |
| D、聚丙烯酸钠是一种体型结构的高分子材料 |
查看答案和解析>>
科目: 来源: 题型:
A、比例模型为: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 | |||
B、2CH3CH2OD+O2
| |||
| C、二氧化硫、氨、煤的液化均为物理变化 | |||
D、实验室中制取乙酸乙酯的方程式为:CH3COOH+H18O-C2H5
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com