
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
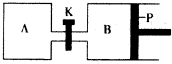 如图所示的装置中发生反应2A2(g)+B2(g)?2C(g);△H=-a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向A,B容器中分别充入2mol A2和1mol B2两容器分别在500℃时达平衡,A中C的浓度为w1 mol/L,放出热量b kJ,B中C的浓度为w2 mol/L,放出热量c kJ.请回答下列问题:
如图所示的装置中发生反应2A2(g)+B2(g)?2C(g);△H=-a kJ/mol(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向A,B容器中分别充入2mol A2和1mol B2两容器分别在500℃时达平衡,A中C的浓度为w1 mol/L,放出热量b kJ,B中C的浓度为w2 mol/L,放出热量c kJ.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:
 (1)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化.实验室用如图装置模拟上述过程:
(1)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化.实验室用如图装置模拟上述过程:查看答案和解析>>
科目: 来源: 题型:

| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
查看答案和解析>>
科目: 来源: 题型:
| c(HCO3-) |
| c(CO32-) |
查看答案和解析>>
科目: 来源: 题型:
 某种对苯二甲酸酯常用作塑料增塑剂,其结构简式如图所示.(R表示相同的烃基)
某种对苯二甲酸酯常用作塑料增塑剂,其结构简式如图所示.(R表示相同的烃基)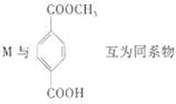

查看答案和解析>>
科目: 来源: 题型:
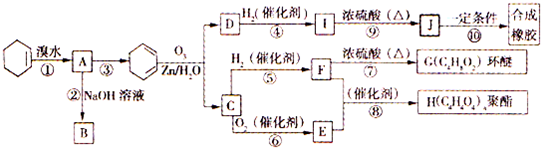
| O3,Zn/H2O |
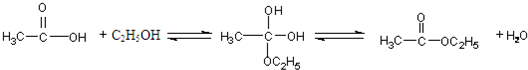
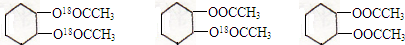 .
.查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com