
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 温度/℃ | 不同压强下的转化率/% | |||
| 0.1MPa | 0.5MPa | 1MPa | 10MPa | |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| 仪器 | 加入试剂 | 作用 |
| A | ||
| E |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
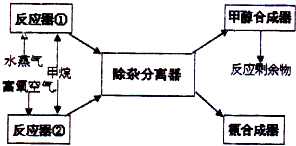 某化工厂以甲烷为主要原料来制取合成甲醇及合成氨的原料,其主要反应为:
某化工厂以甲烷为主要原料来制取合成甲醇及合成氨的原料,其主要反应为:| 2 |
| 3 |
| n(H2) |
| n(N2) |
查看答案和解析>>
科目: 来源: 题型:
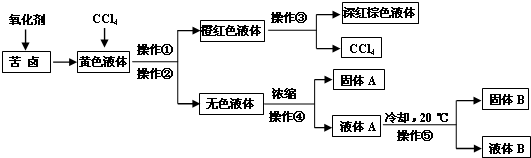

查看答案和解析>>
科目: 来源: 题型:
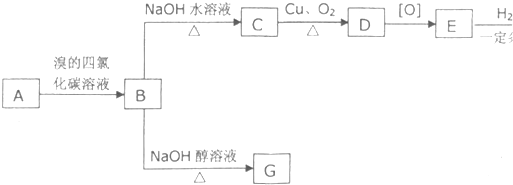
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com