
科目: 来源: 题型:
| 应量取Na2CO3?10H2O的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它玻璃仪器 |
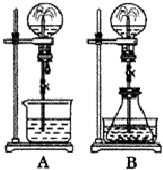 (1)在图A的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体.下列组合中不可能形成喷泉的是
(1)在图A的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体.下列组合中不可能形成喷泉的是查看答案和解析>>
科目: 来源: 题型:
| ||
| ||

| 2 |
| 3 |
查看答案和解析>>
科目: 来源: 题型:
 (1)2005年冬,广东省环保部门监测发现,广东北江韶关段出现了重金属镉超标现象,北江发生严重的水体污染事件,专家确定用1200吨的聚合铁(简称PFS,化学式为:[Fe2(OH)n(SO4)3-
(1)2005年冬,广东省环保部门监测发现,广东北江韶关段出现了重金属镉超标现象,北江发生严重的水体污染事件,专家确定用1200吨的聚合铁(简称PFS,化学式为:[Fe2(OH)n(SO4)3-| n |
| 2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 催化剂 |
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
| 实验编号 | T/℃ | NO初始浓度 ( mol?L-1) |
CO初始浓度 ( mol?L-1) |
催化剂的比表面积 ( m2?g-1) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com