
科目: 来源: 题型:
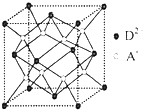 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.请回答下列问题:
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中A+与D2-离子数之比为2:1.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:
 已知KMnO4和H2C2O4(草酸)在酸性溶液中会发生如下反应:
已知KMnO4和H2C2O4(草酸)在酸性溶液中会发生如下反应:| 序号 | A溶液 | B溶液 |
| ① | 2mL0.1mol?L-1 H2C2O4溶液 |
4mL0.01mol?L-1 KMnO4溶液 |
| ② | 2mL0.2mol?L-1 H2C2O4溶液 |
4mL0.01mol?L-1 KMnO4溶液 |
| ③ | 2mL0.2mol?L-1 H2C2O4溶液 |
4mL0.01mol?L-1 KMnO4溶液 少量MnSO4(催化剂) |
查看答案和解析>>
科目: 来源: 题型:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
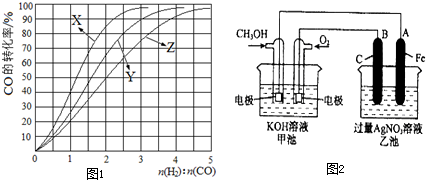
查看答案和解析>>
科目: 来源: 题型:
 SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一.
SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一.| 催化剂 |
| △ |
查看答案和解析>>
科目: 来源: 题型:
| A、该温度下,0.31 mol?L HF溶液的pH=2 |
| B、升高温度或增大浓度,HF的电离平衡常数都将增大 |
| C、两溶液混合后不会产生沉淀 |
| D、向饱和的CaF2溶液中加水后,c(Ca2+)一定比加水前减小 |
查看答案和解析>>
科目: 来源: 题型:
| A、常温下,23gNO2含有nA个氧原子 |
| B、1molFe与足量的稀HNO3反应转移2nA个电子 |
| C、常温常压下,22.4LCCl4含有nA个CCl4分子 |
| D、1molFe2+与 足量H2O2溶液反应,转移2nA个电子 |
查看答案和解析>>
科目: 来源: 题型:
| A、Mg2++2HCO3-+Ca2++2OH-=MgCO3↓+CaCO3↓+2H2O |
| B、Cu2++H2S=Cu S↓+2H+ |
| C、Zn2++S2-+2H2O=Zn(OH)2↓+H2S↑ |
| D、FeS+2H+=Fe2++H2S↑ |
查看答案和解析>>
科目: 来源: 题型:
| 元素代号 | A | B | C | D | E | F |
| 化合价 | -2 | -1 | -2、+6 | +4、-4 | +3 | +1 |
| 原子半径(nm) | 0.074 | 0.099 | 0.102 | 0.117 | 0.143 | 0.186 |
查看答案和解析>>
科目: 来源: 题型:
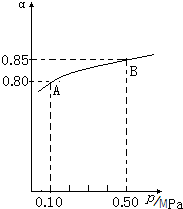
 为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果如图.CO转化率随温度变化的规律是
为了寻找合适的反应温度,研究者进行了一系列试验,每次试验保持原料气组成、压强、反应时间等因素不变,试验结果如图.CO转化率随温度变化的规律是查看答案和解析>>
科目: 来源: 题型:
| A、K+一定存在,Cl-可能存在 |
| B、100 mL溶液中含0.01 mol CO32- |
| C、Cl-一定存在,K+可能存在 |
| D、Ba2+一定不存在,Ca2+可能存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com