
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
- 2 |
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 15 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
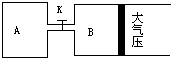 如图所示,当关闭K时,向A中充入4molX、14molY,向B中充入2molX、7molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)?Z(g)+2W(g);△H<0.达到平衡(Ⅰ)时,B中密度变为原来的
如图所示,当关闭K时,向A中充入4molX、14molY,向B中充入2molX、7molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)?Z(g)+2W(g);△H<0.达到平衡(Ⅰ)时,B中密度变为原来的| 10 |
| 9 |
查看答案和解析>>
科目: 来源: 题型:
| 时间/min | CO | Zn | CO2 |
| 0 | 0.11 | 0 | 0 |
| 2 | 0.1 | 0.01 | 0.01 |
| 3 | c1 | c2 | c2 |
| 4 | c1 | c2 | c2 |
查看答案和解析>>
科目: 来源: 题型:
| A、在常温常压下,11.2LN2含有的分子数为0.5NA |
| B、在常温常压下,1molH2含有的原子数为2NA |
| C、0.1mol/LNaCl溶液中含有Na+数目为0.1NA |
| D、在同温同压时,相同体积的任何气体含有相同数目的原子 |
查看答案和解析>>
科目: 来源: 题型:
| A、铁屑溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |
| B、钠与硫酸铜溶液反应:Cu2++2Na=2Na++Cu |
| C、向偏铝酸钠溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D、用双氧水和稀硫酸处理印刷电路板:Cu+H2O2+2H+=Cu2++2H2O |
查看答案和解析>>
科目: 来源: 题型:
| A、含1mol硅原子的SiO2晶体中Si-O键的个数为2NA |
| B、理论上氢氧燃料电池负极消耗11.2L标准状况下气体,外线路通过电子数为NA |
| C、标准状况下,11.2 L氯仿中含有的C-Cl键的数目为1.5NA |
| D、15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com