
科目: 来源: 题型:
| 压强/Mpa 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |

查看答案和解析>>
科目: 来源: 题型:
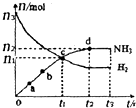 大气固氮属于自然固氮,合成氨是目前人工固氮的主要方法.科学家一直致力“人工固氮”新方法的研究.
大气固氮属于自然固氮,合成氨是目前人工固氮的主要方法.科学家一直致力“人工固氮”新方法的研究.| 反应 | N2+02?2N0 | N2+3H2?2NH3 | ||
| 温度/℃ | 27 | 2000 | 100 | 400 |
| K | 3.84×10-31 | 0.1 | 3.4×109 | 2.0x104 |
| 3 |
| 2 |
查看答案和解析>>
科目: 来源: 题型:
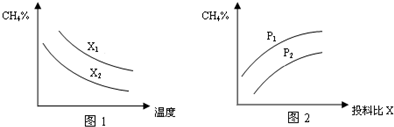 CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物.工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,可以在一定条件下制备甲醇,二甲醚等多种有机物.工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气.| 时间/min 物质 浓度 |
0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2mol?L-1 | 0.13mol?L-1 | 0.1mol?L-1 | 0.1mol?L-1 | 0.09mol?L-1 |
| H2 | 0mol?L-1 | 0.2mol?L-1 | 0.3mol?L-1 | 0.3mol?L-1 | 0.33mol?L-1 |
查看答案和解析>>
科目: 来源: 题型:
 我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用.
我国是世界上发现和使用铜及铜器最早的国家之一,直到现在铜及其化合物在工农业生产中仍然有着广泛的应用.查看答案和解析>>
科目: 来源: 题型:
| A、常温下,2.24LN2和O2的混合气体所含原子数为0.2NA |
| B、常温下,pH=2的醋酸溶液中所含有的H+数为0.01NA |
| C、标准状况下,30g NO和16g O2混合所生成的气体分子数为NA |
| D、标准状况下,6.72L CO2中所含的共用电子对数为1.2NA |
查看答案和解析>>
科目: 来源: 题型:
| A、Ba2+、OH-、NO3-、Na+ |
| B、NH4+、OH-、SO42-、K+ |
| C、Ca2+、H+、Cl-、CO32- |
| D、Cu2+、SO42-、Ba2+、Cl- |
查看答案和解析>>
科目: 来源: 题型:
| A、在0.1 mol?L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| B、在0.1 mol?L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C、向0.2 mol?L-1NaHCO3溶液中加入等体积0.1 mol?L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol?L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
查看答案和解析>>
科目: 来源: 题型:
| 1 |
| 3 |
| A、丙炔 | B、乙炔 | C、乙烯 | D、环丙烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com