
科目: 来源: 题型:
| A、电池总反应的离子方程式为:Mg+H2O2+2H+=Mg2++2H2O |
| B、正极的电极反应为:H2O2+2H++2e-=2H2O |
| C、工作时,正极周围海水的pH减少 |
| D、电池工作时,溶液中的H+向负极移动 |
查看答案和解析>>
科目: 来源: 题型:
| A、①④⑧ | B、①②④ |
| C、①③⑧ | D、①⑤⑦ |
查看答案和解析>>
科目: 来源: 题型:
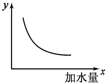 如图表示25℃时,0.1mol/L的一元弱酸HA加水稀释过程中,某量随加水量变化情况,则图中纵坐标y可以是( )
如图表示25℃时,0.1mol/L的一元弱酸HA加水稀释过程中,某量随加水量变化情况,则图中纵坐标y可以是( )| A、溶液的pH | ||
| B、Ka(HA) | ||
C、
| ||
D、
|
查看答案和解析>>
科目: 来源: 题型:
| A、过量SO2通入Ba(NO3)2溶液3SO2+2NO3-+3Ba2++2H2O═3BaSO4+2NO+4H+ | ||
| B、1mol的Cl2通入含1mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 | ||
C、甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH-
| ||
| D、向硫酸铝铵矾溶液中滴加过量的氢氧化钡溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3?H2O+2H2O |
查看答案和解析>>
科目: 来源: 题型:
A、氢氧化钡溶液与稀硫酸:Ba2++2OH-+2H++SO
| ||
B、Al2(SO4)3浴液中加入足量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH
| ||
| C、FeBr2溶液中通入过量Cl2 2Fe2++6Br-+4Cl2=2Fe3++3Br2+8Cl- | ||
| D、Fe2O3溶于过量的盐酸中:Fe2O3+6H+=2Fe3++3H2O |
查看答案和解析>>
科目: 来源: 题型:
| n |
| 2 |
| 3n |
| 2 |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:

| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | |
| 乙 | H2O | 丙 | |||
| 1 | 650 | 4 | 2 | 1.6 | 5 |
| 2 | 900 | 2 | 1 | 0.4 | 3 |
| 3 | 900 | 2 | 1 | 0.4 | 1 |
| 物质 | 乙 | H2O | 丙 | H2 |
| 起始量/mol | 0.8 | 1.0 | 0.6 | 0.8 |
查看答案和解析>>
科目: 来源: 题型:

| T/K | 298 | 398 | 498 |
| K/ | 4.1×106 | K1 | K2 |
查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com