
科目: 来源: 题型:
| A、二氧化硅溶于水显酸性 |
| B、光导纤维传导光的能力非常强,利用光缆通讯,能同时传送大量信息 |
| C、因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强 |
| D、二氧化硅是酸性氧化物,它不溶于任何酸 |
查看答案和解析>>
科目: 来源: 题型:
| A、标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
| B、标准状况下,14 g氮气含有的核外电子数为5NA |
| C、1mol金属钠与氧气反应,不论生成氧化钠还是过氧化钠,转移电子数都是NA |
| D、标准状况下,铝跟氢氧化钠溶液反应生成1 molH2时,转移的电子数为NA |
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 |

查看答案和解析>>
科目: 来源: 题型:
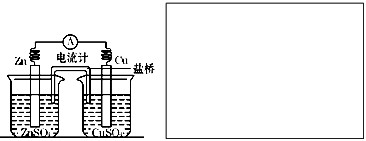
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com